През последните години терапията със стволови клетки се превърна в много обещаваща и напреднала тема на научните изследвания. Развитието на методите на лечение предизвика големи очаквания.
Днес ще се фокусираме върху откриването на различни стволови клетки и потенциалните терапии с тях. Генезисът на стволовите клетки е последван от лабораторни етапи на контролирано култивиране и деривация на стволови клетки. Качественият контрол и анализите за образуване на тератома са важни процедури за оценка на свойствата на тестваните стволови клетки. Методите за извличане и използването на култивиращите среди са от решаващо значение за създаване на подходящи условия на околната среда за контролирана диференциация. Прегледът е обобщен от предизвикателствата, които терапията със стволови клетки трябва да преодолее, за да бъде приета по целия свят. Голямото разнообразие от възможности прави тази авангардна терапия повратна точка в съвременната медицина, осигуряваща надежда за нелечими заболявания. 
Класификация на стволови клетки
Стволовите клетки са неспециализирани клетки на човешкото тяло. Те са в състояние да се диференцират във всяка клетка на организма и имат способността да се самообновяват. Стволовите клетки съществуват както в ембрионите, така и в клетките на възрастните. Има няколко стъпки на специализация. Потенциалността на развитието намалява с всяка стъпка, което означава, че унипотентна стволова клетка не е в състояние да се диференцира в толкова много видове клетки, колкото плурипотентна. Тази глава ще се съсредоточи върху класификацията на стволови клетки, за да улесни читателя да разбере следващите глави.
Тотипотентните стволови клетки са в състояние да се разделят и диференцират в клетки на целия организъм. Тотипотентността има най-висок потенциал за диференциация и позволява на клетките да образуват както ембрионални, така и извънембрионални структури. Един пример за тотипотентна клетка е зигота, която се образува след като сперматозоид опложда яйцеклетка. Тези клетки могат по-късно да се развият или в някой от трите зародишни слоя или да образуват плацента. След приблизително 4 дни вътрешната клетъчна маса на бластоциста става плюрипотентна. Тази структура е източник на плюрипотентни клетки.
Плурипотентните стволови клетки (PSCs) образуват клетки от всички зародишни слоеве, но не и извънембрионални структури, като плацентата. Ембрионалните стволови клетки (ESCs) са пример. ESC се получават от вътрешната клетъчна маса на ембрионите в предимплантацията. Друг пример са индуцирани плюрипотентни стволови клетки (iPSCs), получени от епибластния слой на имплантираните ембриони. Тяхната плурипотентност е континуум, като се започне от напълно плюрипотентни клетки като ESC и iPSC и завършва на представители с по-малка потентност – мулти-, олиго- или унипотентни клетки. Един от методите за оценка на тяхната активност и спектър е анализът за образуване на тератома. iPSC се генерират изкуствено от соматични клетки и функционират подобно на PSC. Тяхното култивиране и използване са много обещаващи за настоящата и бъдещата регенеративна медицина.
Мултипотентните стволови клетки имат по-тесен спектър на диференциация от PSCs, но те могат да се специализират в отделни клетки на специфични клетъчни линии. Един пример е хематопоетична стволова клетка, която може да се развие в няколко типа кръвни клетки. След диференцирането, хематопоетичната стволова клетка се превръща в олигопотентна клетка. След това нейните способности за диференциация се ограничават до клетки от нейния произход. Някои многопотентни клетки обаче са способни да се преобразуват в несвързани типове клетки, което предполага да ги наречем плурипотентни клетки. 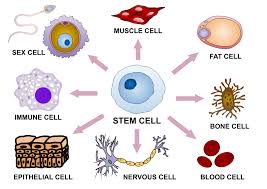
Олигопотентните стволови клетки могат да се диференцират в няколко типа клетки. Миелоидната стволова клетка е пример, който може да се раздели на бели кръвни клетки, но не и червени кръвни клетки.
Унипотентните стволови клетки се характеризират с най-тясната способност за диференциация и специално свойство да се делят многократно. Последната им характеристика ги прави обещаващ кандидат за терапевтична употреба в регенеративната медицина. Тези клетки са в състояние да образуват само един тип клетки, напр. dermatocytes.
Биология на стволовите клетки
След сливането на спермата и яйцеклетката се образува бластоциста. Вътрешната му стена е облицована с краткотрайни стволови клетки, а именно ембрионални стволови клетки. Бластоцистите са съставени от два различни типа клетки: вътрешната клетъчна маса (ICM), която се развива в епибласти и индуцира развитието на плода, и трофектодермата (ТЕ). Бластоцистите са отговорни за регулирането на микросредата ICM. ТЕ продължава да развива и формира извънембрионалните структури за подпомагане, необходими за успешния произход на ембриона, като плацентата. Тъй като ТЕ започва да образува специализирана поддържаща структура, ICM клетките остават недиференцирани, напълно плюрипотентни и пролиферативни. Плурипотентността на стволовите клетки им позволява да образуват всяка клетка на организма. Човешките ембрионални стволови клетки (hESCs) са получени от ICM. По време на процеса на ембриогенезата клетките образуват агрегации, наречени зародишни слоеве: ендодерма, мезодерма и ектодерма, като в крайна сметка всяка от тях поражда диференцирани клетки и тъкани на плода, а по-късно и възрастния организъм. След като hESC се диференцират в един от зародишните слоеве, те се превръщат в многопотентни стволови клетки, чиято потентност е ограничена само до клетките на зародишния слой. Този процес е кратък в човешкото развитие. След това в целия организъм се появяват плюрипотентни стволови клетки като недиференцирани клетки, а основните им способности са пролиферация чрез формиране на следващото поколение стволови клетки и диференциране в специализирани клетки при определени физиологични условия. 
Сигналите, които влияят на процеса на специализация на стволови клетки, могат да бъдат разделени на външни, като физически контакт между клетките или химическа секреция от заобикалящата тъкан, и вътрешни, които са сигнали, контролирани от гени в ДНК.
Стволовите клетки също действат като системи за вътрешно възстановяване на тялото. Попълването и образуването на нови клетки са неограничени, докато организмът е жив. Активността на стволовите клетки зависи от органа, в който се намират; например в костния мозък деленето им е постоянно, въпреки че в органи като панкреаса деленето става само при специални физиологични условия.
Функционално разделение на стволовите клетки
Развитие на цялото тяло
По време на деленето наличието на различни стволови клетки зависи от развитието на организма. Соматичните ESC на стволови клетки могат да бъдат разграничени. Въпреки че извличането на ESC без отделяне от ТЕ е възможно, такава комбинация има граници на растеж. Тъй като разпространяващите действия са ограничени, съвместната култура от тях обикновено се избягва.
ESCs са получени от вътрешната клетъчна маса на бластоциста, която е етап на предварително имплантиране на ембриона около. 4 дни след оплождането. След това тези клетки се поставят в културална чиния, пълна с хранителна среда.
Тези клетки могат да бъдат описани като плюрипотентни, тъй като те могат в крайна сметка да се диференцират във всеки клетъчен тип в организма. От началото на изследванията им съществуват етични ограничения, свързани с медицинската употреба на ESC в терапиите. Повечето ембрионални стволови клетки се развиват от яйцеклетки, които са оплодени в ин витро клиника, а не от естествен процес на оплождане.
Соматичните или възрастни стволови клетки са недиференцирани и се намират сред диференцирани клетки в цялото тяло след развитието. Функцията на тези клетки е да позволяват заздравяването, растежа и подмяната на клетките, които се губят всеки ден. Тези клетки имат ограничен диапазон от възможности за диференциация. Има следните:
- Мезенхимните стволови клетки присъстват в много тъкани. В костния мозък тези клетки се диференцират главно в костните, хрущялните и мастните клетки. Като стволови клетки те са изключение, защото действат плюрипотентно и могат да се специализират в клетките на всеки зародишен слой.
- Невронните клетки пораждат нервни клетки и техните поддържащи клетки – олигодендроцити и астроцити.
- Хематопоетичните стволови клетки образуват всички видове кръвни клетки: червени, бели и тромбоцити.
- Стволовите клетки на кожата образуват например кератиноцити, които образуват защитен слой на кожата.
Времето на пролиферация на соматичните стволови клетки е по-дълго от това на ESC. Възможно е да се препрограмират възрастни стволови клетки обратно в тяхното плурипотентно състояние. Това може да се извърши чрез прехвърляне на възрастното ядро в цитоплазмата на яйцеклетка или чрез сливане с плюрипотентната клетка. Същата техника беше използвана по време на клонирането на известната овца Доли.
HESC участват в развитието на цялото тяло. Те могат да се диференцират в плюрипотентни, тотипотентни, многопотентни и унипотентни клетки.
Плурипотентните клетки могат да бъдат наречени тотипотентни, ако могат допълнително да образуват извънембрионални тъкани на ембриона. Мултипотентните клетки са ограничени при диференциране към всеки тип клетки от дадена тъкан. Когато тъканта съдържа само една линия от клетки, стволовите клетки, които ги образуват, се наричат или олиго- или унипотентни.
Преломна точка в терапията със стволови клетки
Повратният момент в терапията със стволови клетки се появява през 2006 г., когато учените Shinya Yamanaka, заедно с Kazutoshi Takahashi, откриват, че е възможно да се препрограмират многопотентни стволови клетки на възрастни до плюрипотентно състояние. Този процес избягва да застраши живота на плода в процеса. Ретровирус-медиирана трансдукция на миши фибробласти с четири транскрипционни фактора (Oct-3/4, Sox2, KLF4 и c-Myc), които се експресират главно в ембрионални стволови клетки, може да индуцира фибробластите да станат плюрипотентни. Тази нова форма на стволови клетки беше наречена iPSC. Една година по-късно експериментът успя и с човешки клетки . След този успех методът отвори ново поле в изследването на стволови клетки с поколение iPSC линии, които могат да бъдат персонализирани и биосъвместими с пациента. Напоследък изследванията се фокусират върху намаляване на канцерогенезата и подобряване на проводимата система.
Повратният момент беше повлиян от бивши открития, случили се през 1962 и 1987 година.
Предишното откритие се отнася до учения Джон Гурдън, успешно клонирал жаби, като прехвърля ядро от соматичните клетки на жабата в яйцеклетката. Това предизвика пълна реверсия на развитието на соматичните клетки. Резултатите от неговия експеримент станаха огромно откритие, тъй като по- рано се смяташе, че диференцирането на клетките е само еднопосочна улица, но неговият експеримент предполага обратното и демонстрира, че е възможно дори соматична клетка отново да придобие плюрипотентност.
Последното откритие, направено от Дейвис R.L., се фокусира върху изваждането на фибробластната ДНК. Открити са три гена, които първоначално са се появили в миобластите. Принудителната експресия само на един от гените, наречена миогенна диференциация 1 (Myod1), предизвика превръщането на фибробластите в миобласти, показвайки, че е възможно препрограмиране на клетки и дори може да се използва за трансформиране на клетки от една линия в друга.