Както вече знаем , стволовите клетки имат две основни функции: те могат да се самовъзпроизвеждат и могат да се превръщат в различни специализирани видове клетки в зависимост от нуждите ни. Именно това ги прави толкова интересни за медицината.
За щастие, в последните десетилетия има огромен брой утвърдени терапии, а още по- добрата новина е, че има и още прохождащи терапии за някои от най-значимите заболявания. Различните типове стволови клетки подпомагат оздравяването и с отделяните от тях огромна палитра биологично активни молекули – растежни фактори и вещества с противовъзпалително и регенеративно действие. Не напразно терапиите със стволови клетки са една от най- бързо развиващите се сфери на медицината.
Въпреки че стволовите клетки вече се използват успешно в лечението на десетки животозастрашаващи заболявания, внушението, че с тях може да се излекува практически всяка болест, не лежи на научни доказателства и откровено е по-скоро манипулативно.
Размиването на границата между вече утвърдени терапии и такива, които се намират в етап на клинични изпитвания или дори в зоната на научния експеримент, е друга често срещана спекулация по темата, за това днес ще обърнем внимание именно на това.
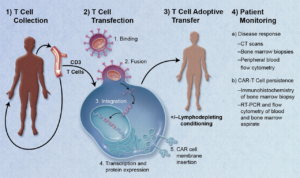
От научен експеримент до клиниката
Както всяко лечение, така и всяка нова клетъчна терапия изминава дълъг път преди да бъде приета, като стандартно лечение. Както и при лекарствата, времето необходимо за дадена диагноза е трудно да бъде предвидено с точност- всичко е свързано не само с научния талант, но и със сериозно финансиране, както и с напредък в разбирането за причините и механизмиет на даденото заболяване.
Нека да видим какви са разликите между експериментални терапии ( предклинични тестове), терапиите в процес на книнични изпитвания и утвърдените терапии ( стандартно лечение).
Експерименталната терапия е лечение, за което учените считат, че би помогнало за лечението на дадено заболяване, но което никога до сега не е било изпитвано върху хора. Експериментите са били или само лабораторни или са били прилагани върху животински модели на даденото заболяване. На такъв етап дадена терапия не може да бъде предвидено, дали и кога ще започне да се изпитва и върху хора и съответно какъв ефект ще има.
Терапиите в процес на клинични изпитвания са строго контролирани и регулирани изследвания за това как влияе дадено ново лечение върху хора. Имат няколко етапа:
- I фаза: оценка на безопасността. Обикновено се прилага върху много малка група хора, доброволци, които са здрави.
- II фаза: изследва задълбочено безопасността и възможните нежелани реакции сред по- голям мащаб , като тук терапията се провежда сред реални болни хора от даденото заболяване.
- III фаза: изследва подробно ефикасността, страничните ефекти и прецизира схемата на лечение , при голям брой пациенти. Всеки един етап от изпитванията може да бъде и ще бъде прекратен в случай, че се появят данни за сериозни рискове.
Утвърдените терапии са следствие на проведени клинични изпитвания с успешен финал. Понякога един такъв процес отнема десетилетия, но въпреки това в днешни дни има над 100 утвърдени терапии със стволови клетки. Този брой се удвоява от 2005 година до сега.
Благодарение на това, че сме съхранили стволови клетки има 30 000 трансплантации на стволвои клетки от пъпна връв от 1988 година до сега.
И когато говорим за видовете терапии със стволови, нека да разгледаме и да отделим кои са утвърдени, кои са в процес на клинично изпитване и кои все още са експериментални.
Утвърдени терапии с хемопоетични стволови клетки:
- Левкемии: остри и хронични левкемии
- Лимфови: Болест на Ходжчкин, Не- Ходжчкинов лимоф, Тумор на Бъркит
- Наследствено аномалии на чревните кръвни клетки- Бета таласемия, вродена еритробластопения, чиста еритроцитна аплазия, сърповидноклетъчна анемия
- Други заболявания на кръвните клетки: Анемии, наследствени аномалии на тромбоцитите, вродени заболявания на имунната система, миелопролиферативни заболявания, наследствени заболявания на имунната система, заболявания свързани с фагоцитите.
- Рак на костния мозък: множествен миелом, плазмоклетъчна левкемия, макроглобулинемия на Уалденстром
- Тумори , с произход различен от кръвотворната система: Невробластом, ретинобластом.
- Вродени заболявания на имунната система и други органи: хрущялно нокътна хипоплазмия, болест на Гюнтер, синдром на сивите тромбоцити, синдром на Пиърсън, синдром на Schwachman, системна мастоцитоза.
- Вродени метаболитни заболявания: мукополизахаридози, левкодистрофии, лизозомни болести на натрупването.
- Други вродени заболявания: синдром на Lesh- Nyhan, остеопороза.
Терпии с хемопоетични стволови клетки в клинично изпитване:
- Автоимунни заболявания: болест на присадката срещу приемника, болест на Крон, диабет тип 1, мултиплена склероза, лупус
- Сърдечно съдови заболявания: инфаркт, възстановяване на сърдечния мускул, исхемия на крайниците, съдови присадки.
- Неврологични заболявания: церебрална парализа, хипоксично- исхемична енцефалопатия, травматично увреждане на мозъка, инсулт, увреждане на гръбначния мозък, амиотрофна латерална склероза, склеродерма, Алцхаймер,дегенеративни състояния.
- Стволовоклетъна и генна терапия при наследствени заболявания ( автоложни): церебрална адренолевкодистрофия, цистична фиброза, анемия на Фанкони, тежък комбиниран имумпдефицит, таласемия,
- Нови приложения: ХИВ
Експериментални терапии с хемопоетични стволови клетки
- Стволовоклетъна и генна терапия при наследствени заболявания: мускулна дистрофия тип Дюшен
- Неврологични заболявания: болест на Алцхаймер, болест на Паркинсон
- Регенеративна медицина: сърце, черен дроб
Важно е да споменем още, че за разлика от хемопоетичните стволови клетки, мезенхимните задължително се подлагат на лабораторно намножаване, тъй като обичайния брой, който може да бъде извлечен е изключително малък. Тази манипулация следователно се извършва под стриктно контролирани условия. Именно за това, мезенхимните стволови клетки биват преравнявани към лекарствените продукти. Право да ги преработват за клинични проучвания имат само специално лицензирани лаборатории ( познати, като клетъчни фабрики) под контрола на лекарствените агенции. В законодателството на Европейския съюз мезенхимните стволови клетки се разглеждат, като лекарствен продукт за модерна терапия ( ATMPs) и са обект на специален Регламент номер 1394/ 2007. В този регламент попадат и хемопоеточните стволови клетки, ако са били подлагани на съществени лабораторни манипулации, като модифициране или размножаване.
Тъканна съвместимост. Какво е това ?
Както знаем, съществуват два типа терапии в зависимост от произхода на стволовите клетки за лечението, а именно автоложна и алогенна. При автоложната, стволовите клетки са предварително отделени от пациента, а при алогенната се използват донорски стволови клетки. И ето тук идва въпроса за тъканната съвместимост.
Когато казваме, че своловите клетки, съхранени при раждането на бебето, имат шанс да се полезни за цялото семейство, не бива да пропускаме факта, че пред използването им за брат или сестра, майка или баща стои едно сериозно препятствие, което трябва да бъде преодоляно: т.нар. тъканна съвместимост.
Става въпрос за кръвногруповите маркери (HLA маркери), с които трябва да се съобразяваме дори, когато говорим за кръвопреливане. Те са своеобразните опознавателни знаци, по които имунната ни система разпознава своето от чуждото, като така ни предпазва непрекъснато от инфекции и ракови клетки. При недостатъчна степен на съвпадение ( както и при трансплантацията на органи) имунната система атакува и унищожава присадката. За разлика от кръвните групи, HLA маркерите са много повече на брой, като с клинично значение са 6 главни позиции, на всяка от които може да има няколко десетки различни варианти. Това е всъщност и причината мнозина болни да чакат с месеци за откриването на съвместим донор, особено ако са представители на по-малки нации или етнически малцинства.
Иначе казано: наследяваме HLA маркерите за тъканна съвместимост в два комплекта (по един от майката и един от бащата).Това означава, че винаги детето е поне 50% съвместимо с всеки от биологичните си родители. Шансът за пълна съвместимост между децата на едни и същи родители е 25%, а 100% гаранция има само и единствено при еднояйчните близнаци.
И тук най- вероятно възниква въпроса, защо тогава да съхраняваме стволови клетки при раждането? Огромното предимство на стволовите клетки, събрани при раждането, в сравнение с тези, получени на по-късен етап от костен мозък или други източници, е че те са имунологично незрели – т.е., техните HLA маркери все още не са експресирани напълно, или казано още по-просто, опознавателните им знаци не са докрай оформени. Това ги прави по-слабо видими за имунната система и позволява една значително по-голяма свобода при употреба със значително по- малък риск от отхвърляне. Тези стволови клетки могат да се използват не само при пълна HLA съвместимост, но и при 5/6 или дори при едва 4/6 съвпадащи HLA маркера – нещо, което е немислимо с клетки от костен мозък.
Поглед назад…
И макар употребата на стволовите клетки в медицината да е изключително нашумяла през последните години, истината е, че всъщност медицината разчита на вълшебните им свойства вече повече от половин век. Всеки път, когато стане въпрос за трансплантация на костен мозък, всъщност става въпрос именно за лечение със стволови клетки. Първата такава операция се случва през далечната 1956 година, а днес стволовоклетъчни трансплантации се извършват над 50 000 пъти годишно. Тогава д-р Едуард Донал Томас успява да постигне пълно излекуване на пациент с остра левкемия, използвайки терапия със стволови клетки от неговия брат близнак. През 1990г. д-р Томас е отличен с Нобелова награда за медицина и така започва една нова епоха в развитието на леченията на едни от най- тежките познати заболявания.
За първи път стволови клетки извлечени от кръв от пъпна връв за лечение са използвани през 1988 година, е сега има вече над 30 000 такива операции. 5 годишния тогава Матю Фароу, става първия човек, който се излекува успешно от анемия на Фанкони, с помощта на стволови клетки от кръв от пъпна връв. Донор на клетките е неговата сестра, а днес Матю е здрав и щастлив млад мъж, който се е посветил на кампании с цел разясняване ползите от стволовите клетки.








